
Kõik iLive'i sisu vaadatakse meditsiiniliselt läbi või seda kontrollitakse, et tagada võimalikult suur faktiline täpsus.
Meil on ranged allhanke juhised ja link ainult mainekate meediakanalite, akadeemiliste teadusasutuste ja võimaluse korral meditsiiniliselt vastastikuste eksperthinnangutega. Pange tähele, et sulgudes ([1], [2] jne) olevad numbrid on nende uuringute linkideks.
Kui tunnete, et mõni meie sisu on ebatäpne, aegunud või muul viisil küsitav, valige see ja vajutage Ctrl + Enter.
Krüptokokk-meningiit
Artikli meditsiiniline ekspert
Viimati vaadatud: 04.07.2025
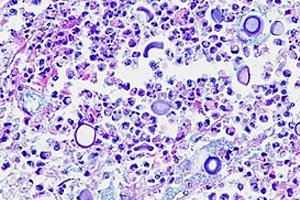
Ajukelmepõletikku võivad põhjustada lisaks bakteritele, viirustele ja protistidele ka seeninfektsioonid. Krüptokokkmeningiiti põhjustab kapseldatud pärmseen Cryptococcus neoformans, mis on inimeste oportunistlik patogeen. [ 1 ] See sai nime Busse-Buschke tõbi Otto Busse ja Abraham Buschke esimese kirjelduse tõttu 1894. aastal. [ 2 ]
RHK-10 kohaselt on haiguskood G02.1 (kesknärvisüsteemi põletikuliste haiguste jaotises) ja mükooside (st seenhaiguste) jaotises ka B45.1.
Epidemioloogia
Kaheksa kümnest krüptokokkmeningiidi juhtumist esineb HIV/AIDSi nakatunud inimestel.
2017. aasta kevadel ajakirjas The Lancet Infectious Diseases avaldatud andmete kohaselt põhjustab seen igal aastal HIV-i või AIDS-i põdevate inimeste seas umbes 220 000 krüptokokkmeningiidi juhtu ja üle 180 000 inimese sureb. Enamik krüptokokkmeningiidi juhtumeid esineb Sahara-taguses Aafrikas.
WHO statistika kohaselt registreeriti 2017. aastal Aafrikas 165,8 tuhat krüptokokkmeningiidi juhtu, Aasia riikides 43,2 tuhat, Põhja- ja Lõuna-Ameerikas 9,7 tuhat ning Euroopa riikides 4,4 tuhat haigusjuhtu.
Põhjused krüptokokk-meningiit
Seda tüüpi meningiidi põhjused on nakatumine seenega Cryptococcus neoformans (klass Tremellomycetes, perekond Filobasidiella), mis elab keskkonnas: pinnases (sh tolmus), mädanenud puidul, lindude (tuvide) ja nahkhiirte väljaheidetes jne. Nakatumine toimub õhu kaudu - seene aerosoolbasidiospooride sissehingamise teel, kuigi enamikul inimestel, kellel on haiguse tekke suhtes piisav immuunsus, C. neoformans ei põhjusta ja jääb fakultatiivseks rakusiseseks oportunistlikuks mikroorganismiks (mis ei saa teisi inimesi nakatada). Loe ka - Krüptokokid - krüptokokoosi tekitajad [ 3 ]
Reeglina tekib krüptokokkmeningiit HIV-positiivsetel inimestel (IVB staadiumis) – sekundaarse infektsioonina, samuti inimestel, kellel on nõrgenenud immuunsüsteem teiste haiguste korral, millega kaasneb pikaajaline immunosupressioon. [ 4 ]
Krüptokokkmeningiiti peetakse krüptokokoosi tserebraalseks või ekstrapulmonaalseks vormiks, mis tekib pärast C. neoformansi hematogeenset levikut hingamisteedest ja kopsudest ajju ja seljaaju.[ 5 ]
Riskitegurid
Krüptokokkmeningiidi tekkeriski suurendavad tegurid on järgmised:
- vastsündinu periood ja imikute enneaegsus;
- immuunsüsteemi nõrgenemine onkoloogilistes haigustes (sh leukeemia, hulgimelanoomi, lümfosarkoomi) HIV-nakkuse ja AIDS-i põdevatel patsientidel;
- diabeet;
- viirushepatiit ja muud immuunkomplekshaigused;
- sirprakuline aneemia;
- keemiaravi onkoloogilise diagnoosi korral;
- ioniseeriva kiirguse lubatud taseme ületamine;
- pikad antibiootikumide või steroidide kuurid;
- intravaskulaarsete kateetrite ja šuntide paigaldamine;
- luuüdi või siseorgani siirdamine.
Pathogenesis
Krüptokokid, mida kaitseb inimese immuunrakkude eest polüsahhariidkapsel (mis pärsib fagotsütoosi), eritavad proteaase, ureaasi, fosfolipaasi ja nukleaasi – ensüüme, mis on võimelised peremeesrakke hävitama. [ 6 ]
Ja krüptokokoosi patogenees seisneb selles, et need ensüümid kahjustavad rakke, lüüsides membraane, modifitseerides molekule, häirides rakuliste organellide funktsioone ja muutes tsütoskeletti. [ 7 ]
Seente seriinproteaasid hävitavad rakuliste valkude peptiidsidemeid, lõhustavad immunoglobuliine ja immuunsüsteemi efektorrakkude valke ning C. neoformansi replikatsioon toimub mononukleaarsetes fagotsüütides (makrofaagides), mis hõlbustab nende levikut. [ 8 ]
Lisaks, läbides endoteelirakke ja kandudes nakatunud makrofaagide sisse, häirivad krüptokokid hematoentsefaalbarjääri (HEB) terviklikkust. Seen levib vereringe kaudu tserebrospinaalvedelikku ja seejärel aju pehmetesse membraanidesse, moodustades ajukoes seenerakkude „kolooniaid“ želatiinsete pseudotsüstide kujul. [ 9 ]
Sümptomid krüptokokk-meningiit
Krüptokokkmeningiidi esimesteks tunnusteks on palavik (temperatuur tõuseb +38,5–39 °C-ni) ja tugevad peavalud.
Kliiniliste sümptomite hulka kuuluvad ka iiveldus ja oksendamine, krambid, kaela jäikus, silmade suurenenud valgustundlikkus ning teadvuse ja käitumise häired. [ 10 ]
Nagu eksperdid märgivad, on meningeaalse sündroomi areng aeglasem kui meninge bakteriaalse infektsiooni korral.
Tüsistused ja tagajärjed
Krüptokoki põhjustatud seenmeningiidi tüsistused ja tagajärjed on:
- koljusisese rõhu märkimisväärne tõus;
- kraniaalnärvide isoleeritud kahjustus koos näonärvi pareesi/halvatuse ja nägemisnärvi atroofiliste muutustega (mis viib oftalmoloogiliste probleemideni);
- põletikulise protsessi levik aju alamkorteksi ja poolkerade kudedesse - krüptokokiline meningoentsefaliit;
- aju abstsessi (krüptokokoomi) teke;
- efusioon subduraalsesse ruumi (aju kõvakesta alla);
- seljaaju vigastus;
- vaimsed muutused ja kognitiivsete funktsioonide langus.
Diagnostika krüptokokk-meningiit
Lisaks haigusloole ja füüsilisele läbivaatusele hõlmab meningiidi korral C. neoformansi infektsiooni diagnoosimine tingimata vereanalüüse: üldist kliinilist ja biokeemilist analüüsi, vereseerumi analüüsi C. neoformansi valkude vastaste antikehade suhtes ja verekultuuri.
Tehakse nimmepunktsioon jatserebrospinaalvedelikust tehakse antigeeni analüüs ning tserebrospinaalvedelikust bakterioskoopiline analüüs (bakterikultuur). [ 11 ]
Instrumentaalne diagnostika viiakse läbi rindkere röntgenograafia ja aju magnetresonantstomograafia abil.
Diferentseeritud diagnoos
Diferentsiaaldiagnoos hõlmab bakteriaalse ja viirusliku etioloogiaga meningiiti ja meningoentsefaliiti, seente Histoplasma capsulatum, Coccidioides immitis, Blastomyces dermatidis või amööbide (sh Naegleria fowleri) põhjustatud ajukahjustusi.
Ravi krüptokokk-meningiit
Etioloogiline ravi on suunatud krüptokokkide hävitamisele, mille puhul kasutatakse seenevastaseid ravimeid.
Raviskeem hõlmab polüeeni seenevastase antibiootikumi amfoteritsiin B (amfotsüül) intravenoosset manustamist (tilguti, tsentraalse veenikateetri kaudu või peritoneaalse infusiooni teel) koos seenevastase ravimiga flutsütosiin (5-fluorotsütosiin) või flukonasool, millel on fungitsiidne ja fungistaatiline toime. Nende ravimite annus arvutatakse sõltuvalt patsiendi kehakaalust.
Patsiendi seisundi pidev jälgimine on vajalik, kuna amfoteritsiin B-l on neerudele toksiline toime ja flutsütosiini kõrvaltoimete hulka võivad kuuluda luuüdi hematopoeetilise funktsiooni pärssimine, hingamisteede või südame seiskumine, nahakahjustuste teke epidermaalse nekrolüüsi kujul jne.
2010. aasta IDSA (Ameerika Nakkushaiguste Ühingu) värskenduses avaldatud soovituste kohaselt ei ole ravi kümne aasta jooksul muutunud. Esmavaliku seenevastane ravi põhineb induktsioonil, konsolideerimisel ja säilitamisel järgmiste kolme tüüpi patsientide puhul: [ 12 ]
HIV-ga seotud haigused
- Induktsioonravi
- Amfoteritsiin B deoksükolaat (0,7–1,0 mg/kg/päevas) + flutsütosiin (100 mg/kg/päevas suukaudselt) 2 nädala jooksul (tõend A1)
- Liposomaalne amfoteritsiin B (3-4 mg/kg/päevas) või lipiidkompleks amfoteritsiin B (5 mg/kg/päevas; neerufunktsiooni jälgimine) + flutsütosiin (100 mg/kg/päevas) 2 nädala jooksul (tõend B2)
- Amfoteritsiin B deoksükolaat (0,7–1,0 mg/kg/päevas) või liposomaalne amfoteritsiin B (3–4 mg/kg/päevas) või amfoteritsiin B lipiidkompleks (5 mg/kg/päevas patsientidele, kes ei talu flutsütosiini) 4–6 nädala jooksul (tõend B2)
- Induktsioonravi alternatiivid
- Amfoteritsiin B deoksükolaat + flukonasool (tõend B1)
- Flukonasool + flutsütosiin (tõend B2)
- Flukonasool (tõend B2)
- Itrakonasool (tõend C2)
- Flukonasool (400 mg/päevas) 8 nädala jooksul (andmed A1)
- Flukonasool (200 mg/päevas) 1 või enama aasta jooksul (tõend A1)
- Itrakonasool (400 mg/päevas) 1 või enama aasta jooksul (tõend C1)
- Amfoteritsiin B deoksükolaat (1 mg/kg/nädalas) 1 või enama aasta jooksul (tõend C1)
- Konsolidatsiooniravi
- Toetav ravi
- Säilitusravi alternatiivid
Siirdamisega seotud haigused
- Induktsioonravi
- Liposomaalne amfoteritsiin B (3-4 mg/kg/päevas) või lipiidkompleks amfoteritsiin B (5 mg/kg/päevas) + flutsütosiin (100 mg/kg/päevas) 2 nädala jooksul (tõend B3)
- Induktsioonravi alternatiivid
- Liposomaalne amfoteritsiin B (6 mg/kg/päevas) või lipiidkompleks amfoteritsiin B (5 mg/kg/päevas) 4-6 nädala jooksul (tõend B3)
- Amfoteritsiin B deoksükolaat (0,7 mg/kg/päevas) 4-6 nädala jooksul (tõend B3)
- Flukonasool (400 kuni 800 mg/päevas) 8 nädala jooksul (tõend B3)
- Flukonasool (200 kuni 400 mg/päevas) 6 kuu kuni 1 aasta jooksul (tõend B3)
- Konsolidatsiooniravi
- Toetav ravi
Mitte-HIV/siirdamisega seotud haigused
- Induktsioonravi
- Amfoteritsiin B deoksükolaat (0,7 kuni 1,0 mg/kg/päevas) + flutsütosiin (100 mg/kg/päevas) 4 või enama nädala jooksul (tõend B2)
- Amfoteritsiin B deoksükolaat (0,7–1,0 mg/kg/päevas) 6 nädala jooksul (tõend B2)
- Liposomaalne amfoteritsiin B (3-4 mg/kg/päevas) või lipiidkompleks amfoteritsiin B (5 mg/kg/päevas) kombinatsioonis flutsütosiiniga, 4 nädalat (tõend B3)
- Amfoteritsiin B deoksükolaat (0,7 mg/kg/päevas) + flutsütosiin (100 mg/kg/päevas) 2 nädala jooksul (tõend B2)
- Konsolidatsiooniravi
- Flukonasool (400 kuni 800 mg/päevas) 8 nädala jooksul (tõend B3)
- Flukonasool (200 mg/päevas) 6–12 kuu jooksul (tõend B3)
- Toetav ravi
Amfoteritsiin B ja flutsütosiini kombinatsioon on osutunud infektsiooni elimineerimisel kõige tõhusamaks ning on näidanud suuremat elulemuse kasu kui amfoteritsiin üksi. Kuid oma hinna tõttu pole flutsütosiin ressurssidega piiratud keskkondades, kus haiguskoormus on suur, sageli saadaval. Amfoteritsiin B ja flukonasooli kombinatsioone on uuritud ning need on näidanud paremaid tulemusi võrreldes ainult amfoteritsiin B-ga.[ 13 ], [ 14 ], [ 15 ]
Ravimata jätmise korral progresseerub kliiniline kulg segasuse, krampide, teadvuse languse ja kooma tekkeni.
Valuvaigistitele allumatu peavalu võib ravida seljaaju dekompressiooniga pärast piisavat neurokuvamisuuringut kompuutertomograafia või magnetresonantstomograafia abil. Ühe nimmepunktsiooniga eemaldatava tserebrospinaalvedeliku ohutu maksimaalne maht on ebaselge, kuid sageli eemaldatakse kuni 30 ml, kontrollides rõhku pärast iga 10 ml eemaldamist.[ 16 ]
Ärahoidmine
Seene Cryptococcus neoformans nakkuse ennetamine on vajalik eelkõige nõrga immuunsüsteemi korral. [ 17 ] Soovitatav on vältida tolmuseid kohti ja mullaga töötamist ning HIV-positiivsed inimesed peaksid saama pidevat retroviirusevastast ravi.
Prognoos
Ilma ravita on mis tahes seenmeningiidi prognoos halb.
Esialgne prognoos sõltub suremuse ennustajatest, näiteks järgmistest [ 18 ], [ 19 ]:
- Tserebrospinaalvedeliku avanemisrõhk on üle 25 cm H2O.
- Madal valgeliblede arv tserebrospinaalvedelikus
- Sensoorne kahjustus
- Hiline diagnoosimine
- Kõrgenenud tserebrospinaalvedeliku antigeeni tiitrid
- Nakkuse kliirensi määr
- Pärmi hulk tserebrospinaalvedelikus ületab 10 mm3 ( tavapärane praktika Brasiilias) [ 20 ]
- HIV-ga mitteseotud patsiendid ja nende patsientide prognostilised tegurid lisaks juba mainitutele:
- Nõrga põletikulise reaktsiooni markerid
- Peavalusid pole
- Primaarne hematoloogiline pahaloomuline kasvaja
- Krooniline neeru- või maksahaigus
Suremus on riigiti erinev, olenevalt ressurssidest. See püsib kõrge Ameerika Ühendriikides ja Prantsusmaal, kus 10-nädalane suremus jääb vahemikku 15–26% ja on HIV-nakkuseta patsientidel veelgi kõrgem hilise diagnoosimise ja düsfunktsionaalsete immuunvastuste tõttu. Teisest küljest suureneb ressursivaestes riikides suremus 10 nädalaga 30%-lt 70%-le hilise pöördumise ning ravimite, vererõhumõõtjate ja optimaalse jälgimise puudumise tõttu.

