
Kõik iLive'i sisu vaadatakse meditsiiniliselt läbi või seda kontrollitakse, et tagada võimalikult suur faktiline täpsus.
Meil on ranged allhanke juhised ja link ainult mainekate meediakanalite, akadeemiliste teadusasutuste ja võimaluse korral meditsiiniliselt vastastikuste eksperthinnangutega. Pange tähele, et sulgudes ([1], [2] jne) olevad numbrid on nende uuringute linkideks.
Kui tunnete, et mõni meie sisu on ebatäpne, aegunud või muul viisil küsitav, valige see ja vajutage Ctrl + Enter.
FDA kiidab Bimzelx'i heaks hidradeniidi raviks
Viimati vaadatud: 02.07.2025
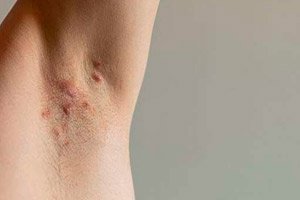 ">
">USA Toidu- ja Ravimiamet (FDA) on heaks kiitnud UCB ravimi Bimzelx (bimekizumab-bkzx) mõõduka kuni raske hidradenitis suppurativa raviks täiskasvanutel.
Bimzelx on esimene ja ainus heakskiidetud ravim, mis lisaks interleukiin 17A-le (IL-17A) selektiivselt inhibeerib ka interleukiin 17F-i (IL-17F). See on Bimzelxi viies näidustus Ameerika Ühendriikides.
Heakskiitmise alus:
Heakskiit põhineb kahe III faasi kliinilise uuringu (BE HEARD I ja BE HEARD II) andmetel, mis viidi läbi mõõduka kuni raske hidradenitis suppurativaga täiskasvanud patsientidel.
Peamine tulemusnäitaja:
- HiSCR50: 16. nädalal saavutas Bimzelxiga ravitud patsientidest platseeboga võrreldes oluliselt suurem osa hidradeniidi suppurativa nähtude ja sümptomite (mõõdetuna hidradeniidi suppurativa kliinilise vastuse (HiSCR50) skoori) ≥50% paranemise.
Teisene indikaator:
- HiSCR75: Ravim andis kliiniliselt olulisi paranemisi ka patsientidel, kes saavutasid 16. nädalal platseeboga võrreldes ≥75% paranemise (HiSCR75).
Tulemuste jätkusuutlikkus:
- Kliiniline ravivastus püsis 48. nädalani ja uusi ohutusalaseid signaale ei tuvastatud.
Eksperdiarvamus:
Dr Alexa B. Kimball, BE HEARD programmi uurija ja dermatoloog Beth Israel Deaconess'i meditsiinikeskuses Bostonis, ütles:
„Bimzelxi heakskiit mõõduka kuni raske hidradenitis suppurativa raviks on oluline areng, arvestades märkimisväärset rahuldamata kliinilist vajadust ja tänapäeval saadaolevate ravivõimaluste piiratud arvu.“
